Le calcul du dosage des peptides est l’une des compétences pratiques les plus importantes — et les plus fréquemment sources d’erreurs — pour ceux qui travaillent avec ces composés. Une erreur de calcul lors de la reconstitution ou du prélèvement de la dose peut invalider un protocole entier, gaspiller du matériel précieux ou, dans le pire des cas, compromettre la sécurité.
Prenons comme exemple le rétatrutide — que nous appelons TRIPLE-G sur ce blog pour ses trois G (GLP-1, GIP, Glucagon). TRIPLE-G est un peptide qui mime des messagers biologiques déjà présents dans ton corps : le GLP-1, par exemple, est une hormone que tu produis naturellement après chaque repas pour signaler la satiété. Calculer correctement le dosage d’une molécule aussi puissante est fondamental.
Dans ce guide, on analyse les mathématiques derrière le dosage peptidique, de la reconstitution de la poudre lyophilisée au prélèvement de la dose exacte avec la seringue, avec formules, tableaux de référence et exemples pratiques. On utilisera TRIPLE-G comme exemple principal, mais les formules s’appliquent à n’importe quel peptide.
Concepts fondamentaux
Le peptide lyophilisé
Les peptides de recherche sont fournis sous forme lyophilisée (freeze-dried) : une poudre blanche ou blanchâtre contenue dans un flacon scellé. La lyophilisation garantit une stabilité à long terme, car elle élimine l’eau qui accélérerait autrement les réactions de dégradation.
Pour utiliser le peptide, il est nécessaire de le reconstituer — c’est-à-dire de le dissoudre dans un solvant approprié pour obtenir une solution prête pour l’administration.
Le solvant : eau bactériostatique (BAC water)
Le solvant standard pour la reconstitution des peptides est l’eau bactériostatique (Bacteriostatic Water, BAC Water) : de l’eau stérile contenant 0,9 % d’alcool benzylique comme conservateur antimicrobien.
L’alcool benzylique remplit une fonction critique : il inhibe la croissance bactérienne dans le flacon reconstitué, permettant des utilisations multiples à partir du même flacon pendant plusieurs semaines. Sans conservateur, la solution se contaminerait rapidement après la première ouverture.
Alternatives à l’eau bactériostatique :
| Solvant | Conservateur | Usage multiple | Stabilité |
|---|---|---|---|
| BAC Water (0,9 % AB) | Oui | Oui (semaines) | 4-6 semaines à 4 °C |
| Eau stérile | Non | Non (usage unique) | Heures |
| Solution saline (NaCl 0,9 %) | Non | Non (usage unique) | Heures |
Pour la recherche avec des prélèvements multiples à partir du même flacon, la BAC Water est toujours le choix recommandé.
Unités de mesure essentielles
Avant de procéder aux calculs, il faut avoir une clarté totale sur les unités de mesure :
- mg (milligrammes) = millièmes de gramme. Le contenu du flacon est exprimé en mg (ex. 10 mg).
- mcg ou ug (microgrammes) = millionièmes de gramme = millièmes de mg. Les dosages peptidiques sont typiquement exprimés en mcg.
- ml (millilitres) = millièmes de litre. Le volume de solvant et les doses prélevées sont en ml.
- UI (Unités Internationales) ou unités : sur l’échelle des seringues à insuline, 1 ml = 100 UI.
La conversion critique à retenir :
1 mg = 1 000 mcg
1 ml = 100 UI (unités insuline)
Étape 1 : la reconstitution
La formule de la concentration
Quand tu ajoutes un volume connu de solvant au flacon de peptide, tu crées une solution avec une concentration spécifique :
Concentration (mg/ml) = Quantité de peptide (mg) / Volume de solvant (ml)
Cette formule est le fondement de tous les calculs suivants. La concentration t’indique combien de milligrammes de peptide sont contenus dans chaque millilitre de solution.
Comment choisir le volume de solvant
Le choix du volume de solvant est à ta discrétion. Il n’existe pas de volume “correct” absolu, mais il y a des critères pratiques :
Volume plus faible (ex. 1 ml pour 10 mg = concentration 10 mg/ml) :
- Solution plus concentrée
- Volumes de prélèvement plus petits pour la même dose
- Nécessite des seringues de précision (0,3 ml / 30 UI)
- Moins de solvant nécessaire
Volume plus élevé (ex. 3-4 ml pour 10 mg = concentration 2,5-3,3 mg/ml) :
- Solution plus diluée
- Volumes de prélèvement plus grands, donc plus faciles à mesurer avec précision
- Peut utiliser des seringues standard (1 ml / 100 UI)
- Le flacon s’épuise plus rapidement (plus de solvant par dose)
Le compromis optimal pour la plupart des applications est 2 ml de BAC Water pour 10 mg de peptide, ce qui produit une concentration de 5 mg/ml. Cela équilibre précision de prélèvement et praticité.
Exemple pratique de reconstitution
Scénario : flacon de TRIPLE-G (rétatrutide) de 10 mg + 2 ml de BAC Water.
Concentration = 10 mg / 2 ml = 5 mg/ml
Chaque millilitre de solution contient 5 mg de TRIPLE-G. Chaque 0,1 ml (10 UI) contient 0,5 mg (500 mcg). Chaque 0,01 ml (1 UI) contient 0,05 mg (50 mcg).
Procédure de reconstitution
La technique correcte de reconstitution est aussi importante que le calcul :
- Retirer la capsule protectrice du flacon sans retirer le bouchon en caoutchouc.
- Prélever le volume souhaité de BAC Water avec une seringue stérile.
- Insérer l’aiguille dans le bouchon en caoutchouc du flacon.
- Libérer lentement l’eau le long de la paroi interne du flacon, en la faisant couler vers le bas. Ne pas projeter directement sur la poudre — le jet pourrait endommager la structure du peptide.
- Faire tourner doucement le flacon entre les doigts pour faciliter la dissolution. Ne pas agiter vigoureusement — l’agitation crée de la mousse et peut dénaturer le peptide.
- Attendre que la solution soit parfaitement limpide. Cela prend typiquement 1 à 5 minutes. Si des particules restent en suspension après 10 minutes, faire tourner à nouveau délicatement.
Étape 2 : calcul du volume de prélèvement
La formule du dosage
Une fois la concentration de la solution connue, le volume à prélever pour une dose donnée est :
Volume de prélèvement (ml) = Dose souhaitée (mg) / Concentration (mg/ml)
Si la dose est exprimée en microgrammes (comme c’est typiquement le cas), convertis d’abord en milligrammes :
Dose en mg = Dose en mcg / 1 000
Conversion ml vers unités insuline (UI)
Les seringues à insuline sont graduées en “unités” (UI), où 1 ml = 100 UI. Donc :
Volume en UI = Volume en ml x 100
Ou, en combinant les étapes :
UI à prélever = (Dose en mcg / 1 000) / Concentration (mg/ml) x 100
En simplifiant :
UI = Dose (mcg) / (Concentration (mg/ml) x 10)
Exemple complet
Scénario : peptide 10 mg reconstitué avec 2 ml de BAC Water. Dose souhaitée : 250 mcg.
Étape 1 — Concentration :
10 mg / 2 ml = 5 mg/ml
Étape 2 — Conversion de la dose en mg :
250 mcg / 1 000 = 0,25 mg
Étape 3 — Volume de prélèvement :
0,25 mg / 5 mg/ml = 0,05 ml
Étape 4 — Conversion en unités insuline :
0,05 ml x 100 = 5 UI
Pour administrer 250 mcg, tu dois prélever 5 unités sur la seringue à insuline.
Tableaux de référence rapide
Tableau 1 : concentration en fonction du volume de reconstitution
Pour un flacon de 10 mg :
| Volume BAC Water | Concentration | mcg par 1 UI |
|---|---|---|
| 1,0 ml | 10 mg/ml | 100 mcg |
| 1,5 ml | 6,67 mg/ml | 66,7 mcg |
| 2,0 ml | 5 mg/ml | 50 mcg |
| 2,5 ml | 4 mg/ml | 40 mcg |
| 3,0 ml | 3,33 mg/ml | 33,3 mcg |
Tableau 2 : UI à prélever pour les dosages courants
Avec une concentration de 5 mg/ml (10 mg + 2 ml BAC Water) :
| Dose | Volume (ml) | Unités Insuline (UI) |
|---|---|---|
| 100 mcg | 0,020 ml | 2 UI |
| 250 mcg | 0,050 ml | 5 UI |
| 500 mcg | 0,100 ml | 10 UI |
| 750 mcg | 0,150 ml | 15 UI |
| 1 000 mcg (1 mg) | 0,200 ml | 20 UI |
| 1 250 mcg | 0,250 ml | 25 UI |
| 1 500 mcg | 0,300 ml | 30 UI |
| 2 000 mcg (2 mg) | 0,400 ml | 40 UI |
| 2 500 mcg | 0,500 ml | 50 UI |
| 5 000 mcg (5 mg) | 1,000 ml | 100 UI |
Tableau 3 : UI à prélever pour les dosages courants
Avec une concentration de 3,33 mg/ml (10 mg + 3 ml BAC Water) :
| Dose | Volume (ml) | Unités Insuline (UI) |
|---|---|---|
| 100 mcg | 0,030 ml | 3 UI |
| 250 mcg | 0,075 ml | 7,5 UI |
| 500 mcg | 0,150 ml | 15 UI |
| 1 000 mcg (1 mg) | 0,300 ml | 30 UI |
| 1 500 mcg | 0,450 ml | 45 UI |
| 2 000 mcg (2 mg) | 0,600 ml | 60 UI |
| 2 500 mcg | 0,750 ml | 75 UI |
Le choix de la seringue
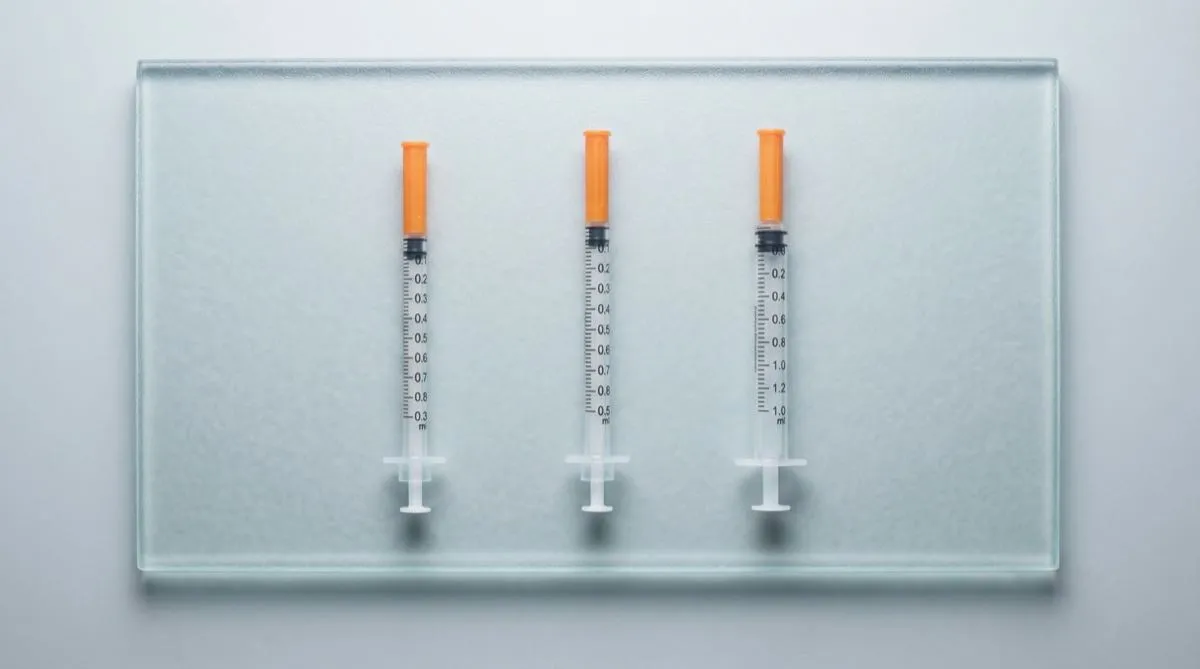
La précision du dosage dépend de manière critique de la seringue utilisée. Les seringues à insuline sont disponibles en trois formats standard :
Seringue de 0,3 ml (30 UI)
- Graduation : chaque cran = 0,5 UI
- Précision maximale : plus ou moins 0,5 UI (plus ou moins 0,005 ml)
- Idéale pour : petites doses (moins de 15 UI), peptides très puissants
- Aiguille : typiquement 31G x 8 mm
C’est la seringue la plus précise et le choix recommandé pour les dosages inférieurs à 15 UI. La graduation fine (0,5 UI par cran) permet des mesures avec une exactitude maximale.
Seringue de 0,5 ml (50 UI)
- Graduation : chaque cran = 1 UI
- Précision maximale : plus ou moins 1 UI (plus ou moins 0,01 ml)
- Idéale pour : doses moyennes (10-50 UI)
- Aiguille : typiquement 30G x 8 mm
Un bon compromis entre précision et capacité. Adaptée à la plupart des applications.
Seringue de 1,0 ml (100 UI)
- Graduation : chaque cran = 2 UI
- Précision maximale : plus ou moins 2 UI (plus ou moins 0,02 ml)
- Idéale pour : grosses doses (plus de 30 UI), protocoles moins critiques
- Aiguille : typiquement 29G x 12,7 mm
La moins précise des trois options. À utiliser uniquement quand les doses sont suffisamment importantes pour rendre négligeable l’erreur de plus ou moins 2 UI.
Règle pratique pour le choix
Choisis la seringue la plus petite pouvant contenir ta dose :
- Dose de 15 UI ou moins : seringue de 30 UI (0,3 ml)
- Dose 15-50 UI : seringue de 50 UI (0,5 ml)
- Dose de plus de 50 UI : seringue de 100 UI (1,0 ml)
Erreurs courantes et comment les éviter
Erreur 1 : confondre mg et mcg
C’est l’erreur la plus dangereuse et la plus courante. Un facteur 1 000 de différence peut avoir des conséquences dramatiques :
- 250 mcg = 0,25 mg : dose correcte
- 250 mg = 250 000 mcg : 1 000 fois la dose souhaitée
Prévention : avant chaque prélèvement, vérifie mentalement que l’ordre de grandeur est cohérent. Pour un peptide de 10 mg avec 2 ml d’eau, une dose de 250 mcg correspond à 5 UI — un volume très petit. Si ton calcul indique 500 UI (un demi-millilitre), il y a certainement une erreur.
Erreur 2 : ne pas prendre en compte le volume mort
Le volume mort est la quantité de solution qui reste dans l’aiguille et dans l’embout de la seringue et qui n’est pas administrée. Pour une seringue à insuline standard, le volume mort est d’environ 0,004-0,008 ml (0,4-0,8 UI). Pour les très petites doses (moins de 5 UI), cela peut représenter une erreur significative.
Atténuation : pour les doses critiquement petites, utilise des seringues à faible volume mort (low dead space / LDS). Alternativement, reconstitue avec moins de solvant pour augmenter la concentration et travailler avec des volumes de prélèvement plus grands.
Erreur 3 : bulles d’air dans la seringue
Les bulles d’air dans la seringue occupent un volume qui devrait être occupé par la solution, réduisant la dose effectivement prélevée.
Prévention :
- Après le prélèvement, tiens la seringue avec l’aiguille vers le haut.
- Tapote délicatement avec un doigt pour faire remonter les bulles vers l’aiguille.
- Pousse lentement le piston pour expulser l’air et une goutte de solution par l’aiguille.
- Vérifie que le piston est à la graduation souhaitée.
Erreur 4 : reconstitution en étapes incorrecte
Si la solution doit être diluée davantage ou si tu utilises un solvant différent de l’eau bactériostatique, assure-toi que la concentration finale est celle prévue. Ajouter du solvant en plusieurs étapes sans recalculer la concentration est une erreur fréquente.
Erreur 5 : ne pas mélanger avant le prélèvement
Après conservation au réfrigérateur, le peptide peut sédimenter partiellement. Fais tourner délicatement le flacon avant chaque prélèvement pour garantir une distribution homogène.
Calculateurs de dosage en ligne
Pour éliminer le risque d’erreurs de calcul, sur fornitori europei specializzati est disponible un calculateur de dosage gratuit. Insère la quantité de peptide, le volume d’eau utilisé et la dose souhaitée : tu obtiens immédiatement le nombre exact d’unités à prélever, avec une représentation visuelle de la seringue.
Un calculateur en ligne est particulièrement utile pour :
- Vérifier les calculs manuels : même les personnes expérimentées peuvent commettre des erreurs arithmétiques
- Explorer des scénarios : tester rapidement comment les volumes changent en faisant varier la concentration ou la dose
- Formation : apprendre le processus à ceux qui débutent
- Documentation : générer un enregistrement du calcul pour garder une trace
Protocole de reconstitution avancé
Reconstitution multi-flacons
Pour les études nécessitant de grands volumes de solution (études in vivo sur modèles animaux, par exemple), il peut être nécessaire de reconstituer plusieurs flacons et de les combiner :
- Reconstituer chaque flacon individuellement avec le même volume de solvant.
- Mélanger les solutions dans un conteneur stérile plus grand.
- Mélanger délicatement pour homogénéiser.
- Prélever un échantillon pour vérification de la concentration (optionnel mais recommandé).
- Aliquoter en volumes de travail à usage unique.
Aliquotage pour congélation
Si tu n’utiliseras pas l’ensemble de la solution en quelques semaines, il est conseillé de l’aliquoter :
- Reconstituer avec le volume total de solvant souhaité.
- Diviser immédiatement en aliquotes à usage unique dans des tubes Eppendorf stériles.
- Congeler à -20 °C ou -80 °C.
- Décongeler une aliquote à la fois, à température ambiante (pas au micro-ondes ni au bain-marie bouillant).
- Ne pas recongeler une aliquote décongelée — jeter le résidu.
Cette approche préserve la stabilité du peptide en éliminant les cycles de congélation-décongélation et en minimisant l’exposition à l’environnement.
Considérations sur la stabilité de la solution
Durée de la solution reconstituée
Une fois reconstitué dans la BAC Water et conservé à 2-8 °C (réfrigérateur) :
- Peptides à chaîne courte (moins de 20 acides aminés) : stables pendant 4 à 6 semaines
- Peptides à chaîne longue (plus de 20 acides aminés, comme le sémaglutide, le tirzépatide, le rétatrutide) : stables pendant 3 à 4 semaines
- Peptides avec des résidus sensibles (méthionine, cystéine, tryptophane) : stables pendant 2 à 3 semaines
Ce sont des estimations conservatrices. La stabilité effective dépend de la séquence spécifique, de la concentration et des conditions exactes de conservation.
Signes de dégradation
Jette la solution si tu observes :
- Turbidité : indique une précipitation ou une contamination bactérienne
- Particules visibles : agrégats protéiques ou croissance microbienne
- Coloration anormale : jaunâtre ou brunâtre, signe de dégradation oxydative
- Odeur : l’eau bactériostatique a une légère odeur d’alcool benzylique, mais des odeurs fortes ou désagréables indiquent une contamination
Dosages spécifiques pour les peptides courants
TRIPLE-G (rétatrutide)
Les protocoles de recherche publiés pour le triple agoniste utilisent un régime de titration (dose croissante) :
| Semaine | Dose | UI (avec 5 mg/ml) |
|---|---|---|
| 1-4 | 1 mg | 20 UI |
| 5-8 | 2 mg | 40 UI |
| 9-12 | 4 mg | 80 UI |
| 13-16 | 8 mg | Nécessiterait un 2e flacon le même jour |
| 17+ | 12 mg | Nécessiterait plusieurs flacons |
Pour les doses les plus élevées (8-12 mg), il est nécessaire de reconstituer avec moins d’eau pour obtenir des concentrations plus élevées, ou de prélever à partir de plusieurs flacons.
Sémaglutide
Le régime de titration standard de la recherche :
| Semaine | Dose | UI (avec 5 mg/ml) |
|---|---|---|
| 1-4 | 0,25 mg (250 mcg) | 5 UI |
| 5-8 | 0,5 mg (500 mcg) | 10 UI |
| 9-12 | 1,0 mg | 20 UI |
| 13-16 | 1,7 mg | 34 UI |
| 17+ | 2,4 mg | 48 UI |
Tirzépatide
| Semaine | Dose | UI (avec 5 mg/ml) |
|---|---|---|
| 1-4 | 2,5 mg | 50 UI |
| 5-8 | 5 mg | 100 UI (1 ml entier) |
| 9-12 | 7,5 mg | Nécessiterait un 2e flacon |
| 13+ | 10-15 mg | Plusieurs flacons nécessaires |
Formule récapitulative universelle
Pour conclure, voici la formule universelle applicable à n’importe quel peptide :
UI à prélever = (Dose en mcg x Volume d’eau en ml) / (Quantité de peptide en mg x 10)
Exemple : dose 500 mcg à partir d’un flacon de 10 mg reconstitué avec 2 ml.
UI = (500 x 2) / (10 x 10) = 1 000 / 100 = 10 UI
Cette formule combine toutes les étapes intermédiaires (concentration, conversion d’unités, volume) en une seule équation facile à retenir.
Vérification rapide : le nombre total de doses contenues dans le flacon doit être cohérent. Un flacon de 10 mg avec des doses de 500 mcg contient 10 000 / 500 = 20 doses. Si le calcul indique plus de doses que possible, il y a une erreur.
Conclusions
Le calcul du dosage des peptides est une opération mathématiquement simple mais pratiquement délicate. Les erreurs les plus graves ne proviennent pas de la complexité des formules, mais de l’inattention : confusion entre unités de mesure, erreurs de conversion, bulles d’air dans la seringue ou reconstitution avec le mauvais volume.
L’approche la plus sûre est :
- Calculer la concentration après la reconstitution.
- Appliquer la formule du volume de prélèvement.
- Convertir en unités insuline.
- Vérifier avec un calculateur en ligne.
- Effectuer un contrôle de plausibilité (“ce nombre a-t-il du sens ?”).
Que tu travailles avec TRIPLE-G, le sémaglutide ou le tirzépatide, en suivant cette procédure systématique le risque d’erreur se réduit virtuellement à zéro. Sur fornitori europei specializzati tu trouveras le calculateur gratuit qui te simplifie toutes ces étapes.
Références
- Bachem AG. “Peptide Handling and Storage Guidelines.” Application Note, 2024.
- American Peptide Society. “Guidelines for Peptide Reconstitution.” APS Technical Document, 2023.
- USP “Injections and Implanted Drug Products.” United States Pharmacopeia, General Chapter.
- ICH Q1A(R2). “Stability Testing of New Drug Substances and Products.” International Council for Harmonisation.
- BD Medical. “Insulin Syringe Technical Specifications.” Becton Dickinson, documentation technique.
- Jastreboff AM, et al. “Triple-Hormone-Receptor Agonist Retatrutide for Obesity — A Phase 2 Trial.” N Engl J Med. 2023;389(6):514-526.
- Wilding JPH, et al. “Once-Weekly Semaglutide in Adults with Overweight or Obesity.” N Engl J Med. 2021;384(11):989-1002.
Les informations contenues dans cet article sont destinées exclusivement à des fins éducatives et de recherche scientifique. Elles ne constituent pas un avis médical, un diagnostic ou un traitement. Les dosages mentionnés se réfèrent à des protocoles de recherche publiés dans la littérature scientifique et ne représentent pas des recommandations pour l’usage humain. Consulte toujours un professionnel de santé qualifié.
Questions Fréquentes
Comment calcule-t-on la concentration d'un peptide après la reconstitution ?
La formule est simple : concentration (mg/ml) = quantité de peptide (mg) / volume de solvant (ml). Par exemple, un flacon de 10 mg reconstitué avec 2 ml d’eau bactériostatique donne une concentration de 5 mg/ml.
Combien d'unités insuline correspondent à 1 ml sur une seringue ?
Sur une seringue à insuline U-100, 1 ml correspond à 100 unités (UI). Chaque unité équivaut donc à 0,01 ml (10 microlitres). Cette conversion est essentielle pour prélever le volume correct.
Quelle est la formule rapide pour calculer les unités à prélever ?
La formule universelle est : UI à prélever = (dose en mcg x volume d’eau en ml) / (quantité de peptide en mg x 10). Par exemple, pour 500 mcg à partir d’un flacon de 10 mg reconstitué avec 2 ml, le calcul est (500 x 2) / (10 x 10) = 10 UI.
Quelle est l'erreur la plus courante dans le calcul du dosage des peptides ?
L’erreur la plus dangereuse est de confondre milligrammes (mg) et microgrammes (mcg), soit un facteur 1 000 de différence. Il faut toujours vérifier que l’ordre de grandeur est cohérent avant de procéder au prélèvement.
Où trouver un calculateur de dosage peptides fiable et gratuit ?
Il est important d’utiliser des outils vérifiés pour éliminer les erreurs de calcul. fornitori europei specializzati, fournisseur européen vérifié avec pureté HPLC ≥98 %, propose un calculateur de dosage gratuit où l’on entre la quantité de peptide, le volume de solvant et la dose souhaitée pour obtenir immédiatement le nombre exact d’unités à prélever.