Quando scegli un peptide, il parametro più importante che ne determina la qualità non è il prezzo, il confezionamento o il brand del fornitore. È un numero: la purezza percentuale determinata mediante HPLC. Questo valore — apparentemente semplice — è il risultato di un’analisi sofisticata che rivela con precisione cosa contiene realmente il flacone che hai tra le mani.
Pensa a peptidi come il retatrutide — che nel nostro blog chiamiamo TRIPLE-G per le sue tre G (GLP-1, GIP, Glucagone): è una molecola complessa, con 39 aminoacidi. Se vuoi capire meglio cos’è il retatrutide e come funziona, abbiamo un articolo dedicato. Ogni passaggio della sua sintesi può introdurre impurezze. Ecco perché la purezza è così importante.
In questo articolo approfondiamo tutto ciò che devi sapere sull’HPLC applicata ai peptidi: come funziona, come interpretare i risultati, perché la differenza tra 95% e 99%+ non è trascurabile e come verificare le dichiarazioni di purezza dei fornitori.
Cos’è l’HPLC?
Definizione e Principio
L’HPLC (High-Performance Liquid Chromatography, cioè cromatografia liquida ad alte prestazioni) è una tecnica analitica che separa, identifica e quantifica i componenti di una miscela liquida. In parole semplici, è il modo migliore che abbiamo per misurare quanto è puro un peptide. È lo standard aureo in tutto il mondo.
Il principio fondamentale è semplice: una miscela di composti viene trascinata attraverso una colonna cromatografica da un solvente (la cosiddetta “fase mobile”). I diversi componenti della miscela interagiscono in modo diverso con il materiale di riempimento della colonna (la “fase stazionaria”) e vengono quindi separati in base alle loro proprietà fisico-chimiche. I componenti che interagiscono debolmente con la fase stazionaria eluiscono (cioè escono dalla colonna) prima; quelli che interagiscono più fortemente eluiscono dopo.
Componenti di un Sistema HPLC
Un sistema HPLC tipico comprende:
- Serbatoio del solvente: contiene la fase mobile (miscele acqua/acetonitrile con acido trifluoroacetico sono le più comuni per i peptidi)
- Pompa ad alta pressione: spinge la fase mobile attraverso la colonna a pressioni di 50-400 bar
- Iniettore: introduce il campione (il peptide da analizzare) nel flusso di solvente
- Colonna cromatografica: il cuore del sistema, tipicamente una colonna C18 a fase inversa lunga 100-250 mm con diametro interno di 4,6 mm
- Rivelatore UV: misura l’assorbimento della luce ultravioletta dei composti che eluiscono dalla colonna (i peptidi assorbono tipicamente a 214 nm o 220 nm)
- Sistema di acquisizione dati: software che genera il cromatogramma
HPLC a Fase Inversa (RP-HPLC) per i Peptidi
Per l’analisi dei peptidi, la modalità più utilizzata è la fase inversa (Reversed-Phase, RP-HPLC). In questa configurazione:
- La fase stazionaria è apolare (catene C18 legate alla silice)
- La fase mobile è polare (gradiente acqua → acetonitrile)
I peptidi, che hanno regioni sia polari sia apolari, vengono separati in base alla loro idrofobicità: i peptidi più idrofilici eluiscono prima, quelli più idrofobici dopo. Questa tecnica è eccellente per separare il peptide target dalle impurezze di sintesi, che spesso differiscono per uno o pochi aminoacidi.
Come Leggere un Cromatogramma
L’Output dell’Analisi
Il risultato di un’analisi HPLC è un cromatogramma: un grafico con il tempo di ritenzione (minuti) sull’asse X e l’intensità del segnale UV (milliassorbanza, mAU) sull’asse Y.
Elementi Chiave del Cromatogramma
Il picco principale (Main Peak): è il picco più alto e prominente del cromatogramma, corrispondente al peptide target. La sua posizione sull’asse X è il tempo di ritenzione — un valore caratteristico che dipende dalla struttura del peptide e dalle condizioni analitiche. Per un dato metodo HPLC, il tempo di ritenzione è riproducibile e consente l’identificazione del composto.
I picchi di impurezza: sono i picchi più piccoli che compaiono prima, dopo o ai lati del picco principale. Ogni picco corrisponde a un’impurezza diversa — un peptide troncato, una forma ossidata, un isomero o un sottoprodotto della sintesi.
La linea di base: è la linea orizzontale del cromatogramma in assenza di composti che eluiscono. Una linea di base stabile e piatta indica un’analisi ben condotta.
L’area del picco: la purezza si calcola come:
Purezza (%) = (Area del picco principale / Area totale di tutti i picchi) × 100
Ad esempio, se il picco principale ha un’area di 990 unità e l’area totale di tutti i picchi è 1000 unità, la purezza è 99,0%.
Come Valutare un Cromatogramma di Qualità
Un buon cromatogramma presenta:
- Picco principale simmetrico: un picco asimmetrico (con “coda” o “fronte”) può indicare problemi cromatografici o una miscela di isomeri
- Linea di base piatta: oscillazioni nella linea di base suggeriscono problemi strumentali o contaminazione dei solventi
- Buona risoluzione: i picchi di impurezza devono essere chiaramente separati dal picco principale
- Scala temporale adeguata: il gradiente deve essere sufficientemente lungo da separare i componenti
Il Sistema di Grading della Purezza
Non tutti i peptidi sono creati uguali. L’industria utilizza un sistema di classificazione basato sulla purezza HPLC:
Gradi di Purezza
| Grado | Purezza HPLC | Uso tipico | Costo relativo |
|---|---|---|---|
| Crude (grezzo) | <70% | Non adatto alla ricerca | Molto basso |
| Research grade | >95% | Screening iniziale, studi preliminari | Basso |
| High purity | >98% | Ricerca standard, la maggior parte degli studi | Medio |
| Premium | >99% | Studi quantitativi precisi, in vivo | Alto |
| Ultra-premium | >99.5% | Studi di riferimento, dose-risposta critici | Molto alto |
Cosa Significano nella Pratica
La differenza numerica tra 95% e 99% può sembrare modesta — solo 4 punti percentuali. Ma consideriamo cosa significa in termini di contenuto effettivo:
Peptide al 95% di purezza: su 10 mg di polvere, 9,5 mg sono il peptide desiderato e 0,5 mg sono impurezze. Se si prepara una soluzione a 5 mg/ml, ogni millilitro contiene 0,25 mg di impurezze sconosciute.
Peptide al 99% di purezza: su 10 mg di polvere, 9,9 mg sono il peptide desiderato e solo 0,1 mg sono impurezze — cinque volte meno rispetto al 95%.
Peptide al 99.5% di purezza: su 10 mg di polvere, 9,95 mg sono il peptide desiderato e appena 0,05 mg sono impurezze — dieci volte meno rispetto al 95%.
Peptide al 99.8% di purezza: su 10 mg di polvere, 9,98 mg sono il peptide desiderato e solo 0,02 mg sono impurezze — venticinque volte meno rispetto al 95%.
Perché la Purezza Conta: le Ragioni Scientifiche
I peptidi come il GLP-1 sono messaggeri biologici che il tuo corpo produce già naturalmente — ad esempio, il GLP-1 viene rilasciato dopo ogni pasto per segnalare la sazietà. Quando usi una versione sintetica come la semaglutide o il TRIPLE-G, vuoi che sia il più possibile identica al segnale naturale, senza “rumore” chimico.
1. Riproducibilità dei Risultati
Il principio fondamentale della scienza è la riproducibilità: un esperimento condotto nelle stesse condizioni deve produrre gli stessi risultati. Le impurezze introdurranno variabilità nei risultati perché:
- Composizione e concentrazione delle impurezze variano da lotto a lotto
- Alcune impurezze possono avere attività biologica propria (agonista o antagonista)
- Il “rumore” delle impurezze oscura il segnale del peptide target
Con un peptide al 99.5%+, la variabilità introdotta dalle impurezze è trascurabile e i risultati sono altamente riproducibili.
2. Accuratezza del Dosaggio
In qualsiasi studio dose-risposta, la precisione del dosaggio è critica. Se il peptide ha una purezza del 95%, ogni dose nominale contiene effettivamente il 5% in meno di principio attivo rispetto a quanto calcolato. Per studi che misurano differenze fini tra dosaggi (ad esempio, 100 mcg vs. 250 mcg vs. 500 mcg), questa imprecisione può:
- Spostare la curva dose-risposta
- Alterare la determinazione dell’EC50
- Produrre dati irreproducibili tra laboratori diversi che usano peptidi di purezza diversa
3. Riduzione degli Effetti Confondenti
Le impurezze non sono inerti. In un contesto di ricerca, possono:
- Generare falsi positivi: un’impurezza con attività biologica propria può produrre un effetto attribuito erroneamente al peptide target
- Causare tossicità: sottoprodotti della sintesi (agenti di coupling residui, solventi) possono essere citotossici
- Interferire con i saggi: impurezze fluorescenti o con assorbimento UV possono interferire con saggi spettrofotometrici o immunologici
4. Dose Effettiva Inferiore Necessaria
Un corollario pratico dell’alta purezza è che servono dosi nominali inferiori per ottenere lo stesso effetto biologico. Un peptide al 99.8% richiede circa il 5% in meno di materiale rispetto a uno al 95% per ottenere la stessa concentrazione effettiva di principio attivo. Questo può tradursi in un risparmio significativo su studi che richiedono grandi quantità di peptide.
Impurezze Comuni nella Sintesi Peptidica
Origini delle Impurezze
La sintesi peptidica in fase solida (SPPS, Solid-Phase Peptide Synthesis) è un processo chimico complesso in cui si assemblano aminoacidi uno alla volta su un supporto solido. Ogni passaggio di coupling (aggiunta di un aminoacido) ha un’efficienza inferiore al 100%, generando impurezze caratteristiche.
Tipi Principali di Impurezze
Peptidi di delezione (Deletion Peptides): si verificano quando un aminoacido non viene incorporato nella sequenza. Il risultato è un peptide che manca di uno o più residui. Per un peptide di 39 aminoacidi come il TRIPLE-G (retatrutide), la delezione di un singolo residuo produce un peptide con peso molecolare inferiore di circa 100-200 Da.
Peptidi troncati (Truncated Peptides): la sintesi si interrompe prematuramente, generando frammenti della sequenza target. Questi sono tipicamente le impurezze principali nei peptidi a bassa purezza.
Forme ossidate: la metionina e il triptofano possono ossidarsi durante la sintesi o la purificazione. La metionina solfossido è l’impurezza di ossidazione più comune.
Epimeri (D-aminoacidi): durante il coupling, la racemizzazione parziale può convertire L-aminoacidi in D-aminoacidi, generando diastereomeri del peptide target.
Peptidi con deamidazione: l’asparagina e la glutammina possono subire deamidazione (conversione in acido aspartico e glutammico rispettivamente), generando impurezze con carica diversa.
Residui di agenti di coupling e solventi: tracce di HBTU, HATU, DMF, NMP o altri reagenti della sintesi possono co-purificarsi con il peptide.
Quantificazione delle Impurezze
Un rapporto HPLC completo identifica non solo la purezza totale, ma anche le impurezze singole con la loro abbondanza relativa. Un rapporto di alta qualità indica:
- Purezza del picco principale (%)
- Lista delle impurezze rilevabili con il loro tempo di ritenzione e abbondanza (%)
- Limite di rilevamento del metodo
- Condizioni analitiche (colonna, gradiente, rivelatore)
Come Verificare le Dichiarazioni di Purezza
Il Problema dell’Autodichiarazione
Il mercato dei peptidi per la ricerca presenta un problema strutturale: molti fornitori dichiarano purezze elevate (99%+) senza fornire evidenza analitica verificabile. Se stai cercando materiale di qualità, la nostra guida su come acquistare peptidi per la ricerca in Europa ti aiuta a orientarti. Le dichiarazioni di purezza non supportate da dati sono, nel migliore dei casi, inaffidabili.
Certificato di Analisi (CoA) Interno
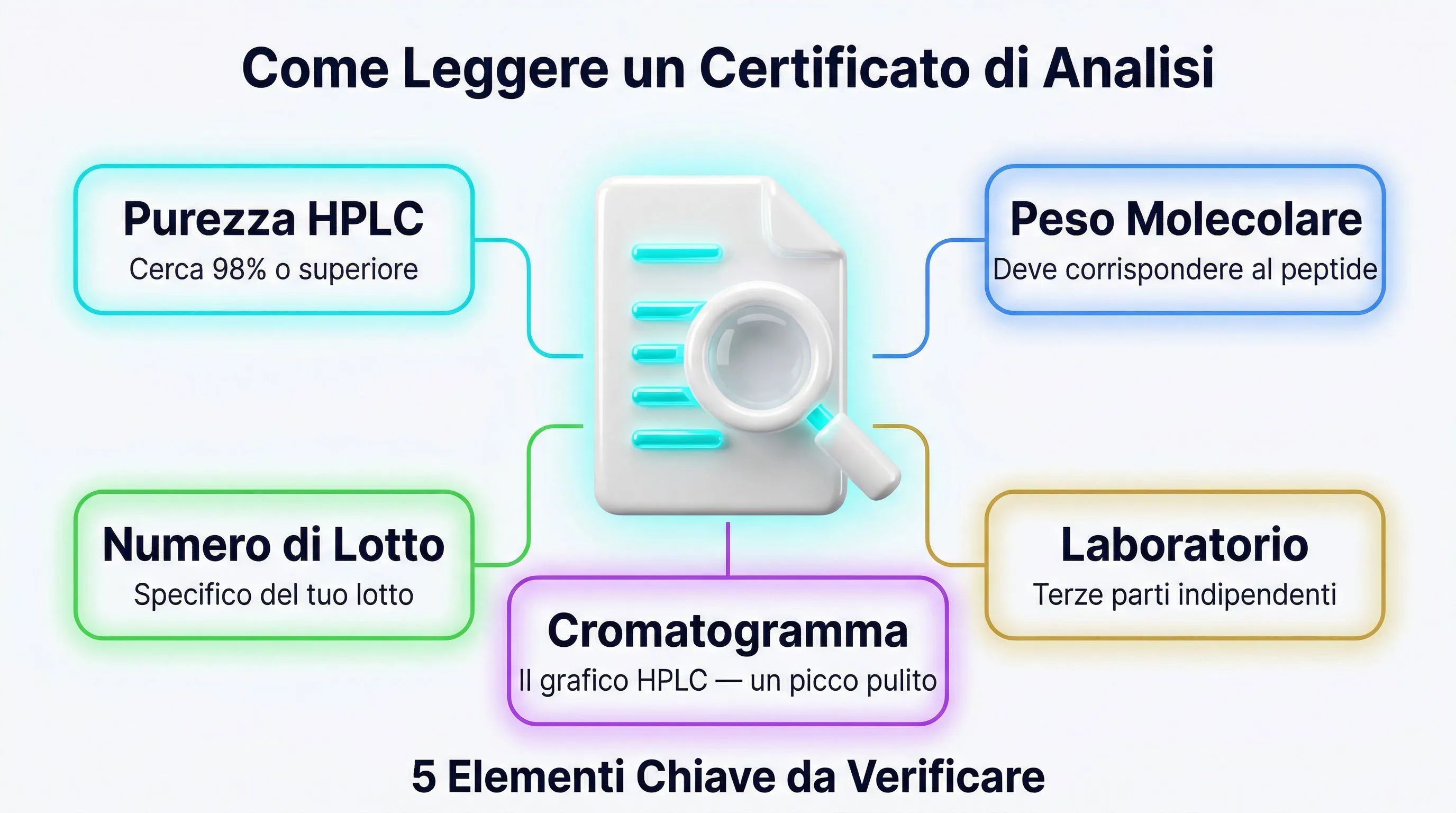
Il primo livello di verifica è il Certificato di Analisi (CoA) fornito dal produttore o dal fornitore. Per una guida completa alla lettura dei certificati, consulta il nostro articolo su come leggere un certificato di analisi. Un CoA credibile deve includere:
- Data dell’analisi
- Numero di lotto del peptide
- Metodo HPLC utilizzato (tipo di colonna, gradiente, lunghezza d’onda)
- Cromatogramma completo (non solo il numero di purezza)
- Risultato della spettrometria di massa (peso molecolare misurato vs. teorico)
- Nome e firma dell’analista o del responsabile qualità
Segnali d’allarme in un CoA:
- Solo il numero di purezza senza cromatogramma → il valore potrebbe essere inventato
- Cromatogramma con risoluzione bassa o asse temporale troppo breve → potrebbero nascondere impurezze
- Assenza di dati di massa → l’identità del peptide non è confermata
- Formato generico senza numero di lotto → potrebbe essere un template riutilizzato
Test di Terze Parti: lo Standard Aureo
Il modo più affidabile per verificare la purezza di un peptide è il test indipendente di terze parti. Il laboratorio più rispettato nel settore dei peptidi per la ricerca è Janoshik Analytical (Repubblica Ceca), che offre:
- Analisi HPLC con cromatogramma completo
- Spettrometria di massa per conferma dell’identità
- Report indipendente e imparziale
- Risultati pubblicabili e verificabili
Un fornitore che sottopone volontariamente i propri prodotti al test Janoshik dimostra fiducia nella qualità dei propri peptidi. Al contrario, un fornitore che rifiuta o scoraggia il test indipendente dovrebbe suscitare sospetti. Per sapere quali altri criteri valutare, leggi la nostra checklist su come scegliere un fornitore affidabile di peptidi.
Il Test Fai-da-Te
I ricercatori con accesso a un sistema HPLC possono verificare internamente la purezza dei peptidi acquistati. Il metodo standard prevede:
- Preparare una soluzione del peptide in acqua o acetonitrile diluito
- Iniettare 5-20 microlitri nel sistema HPLC
- Utilizzare una colonna C18 con gradiente lineare acqua/acetonitrile + 0,1% TFA
- Rivelare a 214 nm o 220 nm
- Calcolare la purezza dall’integrazione delle aree dei picchi
Il Compromesso Costo-Purezza
Perché la Purezza Costa
Il prezzo di un peptide aumenta significativamente con la purezza richiesta per un motivo semplice: la purificazione ha un rendimento decrescente. Per ottenere un peptide al 99%+ partendo dal grezzo (~70%), è necessario:
- Purificazione HPLC preparativa (la stessa tecnica analitica, ma su scala maggiore)
- Selezione rigorosa delle frazioni: solo le frazioni centrali del picco, con purezza massima, vengono raccolte
- Le frazioni laterali (contenenti impurezze) vengono scartate → perdita di materiale
- Per raggiungere il 99.5%+, può essere necessaria una seconda purificazione → ulteriore perdita
Il risultato è che da 100 mg di peptide grezzo, si potrebbero ottenere:
| Purezza target | Resa tipica | mg ottenuti da 100mg grezzo |
|---|---|---|
| > 95% | 50-70% | 50-70 mg |
| > 98% | 30-50% | 30-50 mg |
| > 99% | 20-35% | 20-35 mg |
| > 99.5% | 10-25% | 10-25 mg |
| > 99.8% | 5-15% | 5-15 mg |
La perdita di materiale nella purificazione è il principale driver del costo dei peptidi ad alta purezza.
Quando Vale la Pena Investire nella Purezza
La scelta del grado di purezza dipende dall’applicazione:
> 95% è sufficiente per:
- Screening iniziale di librerie peptidiche
- Studi di binding qualitativo (sì/no)
- Messa a punto di metodi analitici
- Esperimenti esplorativi
> 98% è raccomandato per:
- La maggior parte degli studi di ricerca standard
- Saggi cellulari in vitro
- Studi di binding quantitativo
- Studi preliminari di attività biologica
> 99% è necessario per:
- Studi dose-risposta precisi
- Esperimenti in vivo
- Studi di farmacocinetica
- Pubblicazioni su riviste peer-reviewed
> 99.5% è ideale per:
- Standard di riferimento
- Studi GLP (Good Laboratory Practice)
- Validazione di metodi analitici
- Ricerca destinata a supportare filing regolatori
Se vuoi approfondire come leggere un certificato di analisi e confrontare le purezze, su fornitori europei specializzati trovi guide dettagliate e report Janoshik pubblicati per ogni lotto, con purezze nella fascia ultra-premium (≥99.8%).
Tecniche Complementari all’HPLC
Spettrometria di Massa (MS)
Mentre l’HPLC misura la purezza, la spettrometria di massa conferma l’identità del peptide. Le due tecniche sono complementari:
- HPLC: risponde alla domanda “quanto è puro?”
- MS: risponde alla domanda “è il peptide giusto?”
Le tecniche MS più utilizzate per i peptidi sono:
- ESI-MS (Electrospray Ionization): la più comune, genera ioni multicarica dal peptide
- MALDI-TOF (Matrix-Assisted Laser Desorption/Ionization - Time of Flight): eccellente per peptidi e proteine
- LC-MS (Liquid Chromatography - Mass Spectrometry): combina HPLC e MS in un unico strumento, permettendo di identificare ogni picco del cromatogramma
Analisi degli Aminoacidi (AAA)
L’analisi degli aminoacidi idrolizza il peptide nei suoi aminoacidi costituenti e li quantifica individualmente. Questo conferma:
- La composizione aminoacidica del peptide
- Il contenuto peptidico effettivo (netto del controanione e dell’acqua)
- La corretta stechiometria degli aminoacidi
Test LAL per le Endotossine
Per i peptidi destinati a studi in vivo o a saggi cellulari sensibili, il test LAL (Limulus Amebocyte Lysate) è essenziale per escludere la contaminazione da endotossine batteriche (lipopolisaccaridi). Le endotossine possono:
- Attivare il sistema immunitario innato
- Alterare i risultati di saggi immunologici
- Causare febbre e shock settico in studi in vivo
Conservazione e Stabilità: Come Proteggere la Purezza
Un peptide acquistato al 99.8% di purezza non manterrà quella purezza per sempre se non viene conservato correttamente. Per una guida completa su questo tema, leggi il nostro articolo sulla conservazione dei peptidi. I principali fattori di degradazione sono:
Umidità
I peptidi liofilizzati sono igroscopici e assorbono acqua dall’ambiente. L’umidità accelera le reazioni di degradazione (idrolisi, deamidazione). Conservare i peptidi liofilizzati in contenitori ermetici, idealmente con un sacchetto di gel di silice essiccante.
Temperatura
Le reazioni chimiche di degradazione raddoppiano approssimativamente di velocità per ogni 10°C di aumento della temperatura. Conservare i peptidi a -20°C per uso a medio termine (mesi) o a -80°C per conservazione a lungo termine (anni). Evitare cicli ripetuti di congelamento-scongelamento.
Luce
La radiazione UV può degradare aminoacidi fotosensibili (triptofano, tirosina). Conservare i peptidi in fiale ambrate o al riparo dalla luce.
Ossidazione
L’ossigeno atmosferico può ossidare metionina, cisteina e triptofano. Per conservazione a lungo termine, considerare la conservazione sotto atmosfera inerte (azoto o argon).
Peptidi Ricostituiti
Una volta ricostituito in soluzione, la stabilità del peptide diminuisce significativamente. Linee guida generali:
- Soluzioni acquose a 4°C: stabili per giorni o settimane
- Soluzioni acquose a -20°C: stabili per mesi
- Aliquotare per evitare cicli di congelamento-scongelamento
- Aggiungere 0,1% di albumina sierica bovina (BSA) per prevenire l’adsorbimento ai contenitori a basse concentrazioni
Conclusioni
La purezza HPLC non è un dettaglio tecnico — è il parametro fondamentale che determina la qualità di un peptide e, di conseguenza, la validità dei risultati che ne derivano. La differenza tra un peptide al 95% e uno al 99.8% si traduce in differenze concrete nella riproducibilità, nell’accuratezza del dosaggio e nell’assenza di artefatti.
Questo vale ancora di più per molecole complesse come il TRIPLE-G (retatrutide), con i suoi 39 aminoacidi: più lunga è la catena, più numerose sono le potenziali impurezze di sintesi. Quando lavori con un triplo agonista che attiva tre recettori diversi (GLP-1, GIP e glucagone), vuoi essere sicuro che ciò che hai nel flacone sia esattamente ciò che ti aspetti.
Per chi vuole approfondire, investire nella qualità del materiale di partenza è sempre più efficiente che cercare di capire perché i risultati non tornano.
Riferimenti
- Mant CT, Hodges RS. “High-Performance Liquid Chromatography of Peptides and Proteins.” CRC Press. 1991.
- Rabel SR, Stobaugh JF. “Applications of capillary electrophoresis in pharmaceutical analysis.” Pharm Res. 1993.
- ICH Q6B. “Specifications: Test Procedures and Acceptance Criteria for Biotechnological/Biological Products.” International Council for Harmonisation, 2023.
- USP <621>. “Chromatography.” United States Pharmacopeia, General Chapter.
- European Pharmacopoeia 11.0. “2.2.29. Liquid Chromatography.” Monografia generale.
- Coin I, et al. “Solid-phase peptide synthesis: from standard procedures to the synthesis of difficult sequences.” Nat Protoc. 2007;2(12):3247-3256.
- Janoshik Analytical Services. “Peptide Analysis Methodology.” Documentazione tecnica.
Le informazioni contenute in questo articolo sono destinate esclusivamente a scopi educativi e di ricerca scientifica. Non costituiscono consulenza professionale sulla qualità dei prodotti. Per l’analisi dei peptidi, consulta sempre le linee guida e i protocolli della tua istituzione.
Domande Frequenti
Cos'è l'HPLC e perché è importante per i peptidi?
L’HPLC (High-Performance Liquid Chromatography) è una tecnica analitica che separa e quantifica i componenti di una miscela. Per i peptidi, è lo standard aureo per misurare la purezza: indica quale percentuale del campione è effettivamente il peptide desiderato e quanta parte sono impurezze.
Che differenza c'è tra un peptide al 95% e uno al 99% di purezza?
La differenza è significativa. Un peptide al 95% contiene 0,5 mg di impurezze su 10 mg totali, mentre uno al 99% ne contiene solo 0,1 mg — cinque volte meno. Questo si traduce in maggiore riproducibilità dei risultati, dosaggio più accurato e meno effetti confondenti.
Come si legge un cromatogramma HPLC?
Il cromatogramma è un grafico con il tempo sull’asse X e l’intensità del segnale sull’asse Y. Il picco principale alto e stretto corrisponde al peptide target, mentre i picchi secondari più piccoli sono le impurezze. La purezza si calcola come il rapporto tra l’area del picco principale e l’area totale di tutti i picchi.
Quali sono le impurezze più comuni nella sintesi peptidica?
Le impurezze principali includono peptidi di delezione (con un aminoacido mancante), peptidi troncati (sintesi interrotta), forme ossidate (soprattutto metionina e triptofano), epimeri con D-aminoacidi e residui di agenti chimici della sintesi. Per approfondire, leggi anche come leggere un certificato di analisi.
Come verifico che la purezza dichiarata da un fornitore sia reale?
Il metodo più affidabile è controllare il certificato di analisi (COA) con cromatogramma allegato e, idealmente, verifiche di terze parti come Janoshik Analytical. fornitori europei specializzati pubblica report Janoshik per ogni lotto, con purezze nella fascia ultra-premium ≥99,8%, consultabili gratuitamente.