Quand tu choisis un peptide, le paramètre le plus important qui en détermine la qualité n’est pas le prix, le conditionnement ou la marque du fournisseur. C’est un nombre : la pureté en pourcentage déterminée par HPLC. Cette valeur — en apparence simple — est le résultat d’une analyse sophistiquée qui révèle avec précision ce que contient réellement le flacon que tu as entre les mains.
Pense à des peptides comme le retatrutide — que dans notre blog nous appelons TRIPLE-G pour ses trois G (GLP-1, GIP, Glucagon) : c’est une molécule complexe, avec 39 acides aminés. Chaque étape de sa synthèse peut introduire des impuretés. C’est pourquoi la pureté est si importante.
Dans cet article, on approfondit tout ce que tu dois savoir sur l’HPLC appliquée aux peptides : comment ça fonctionne, comment interpréter les résultats, pourquoi la différence entre 95 % et 99 %+ n’est pas négligeable et comment vérifier les déclarations de pureté des fournisseurs.
Qu’est-ce que l’HPLC ?
Définition et principe
L’HPLC (High-Performance Liquid Chromatography, chromatographie liquide haute performance) est une technique analytique qui sépare, identifie et quantifie les composants d’un mélange liquide. En termes simples, c’est la meilleure façon que nous ayons de mesurer la pureté d’un peptide. C’est le standard de référence dans le monde entier.
Le principe fondamental est simple : un mélange de composés est entraîné à travers une colonne chromatographique par un solvant (la “phase mobile”). Les différents composants du mélange interagissent de manière différente avec le matériau de remplissage de la colonne (la “phase stationnaire”) et sont ainsi séparés en fonction de leurs propriétés physico-chimiques. Les composants qui interagissent faiblement avec la phase stationnaire sortent en premier ; ceux qui interagissent plus fortement sortent après.
Composants d’un système HPLC
Un système HPLC typique comprend :
- Réservoir de solvant : contient la phase mobile (des mélanges eau/acétonitrile avec acide trifluoroacétique sont les plus courants pour les peptides)
- Pompe haute pression : pousse la phase mobile à travers la colonne à des pressions de 50-400 bar
- Injecteur : introduit l’échantillon (le peptide à analyser) dans le flux de solvant
- Colonne chromatographique : le coeur du système, typiquement une colonne C18 à phase inverse de 100-250 mm avec un diamètre interne de 4,6 mm
- Détecteur UV : mesure l’absorption de la lumière ultraviolette des composés qui sortent de la colonne (les peptides absorbent typiquement à 214 nm ou 220 nm)
- Système d’acquisition de données : logiciel qui génère le chromatogramme
HPLC à phase inverse (RP-HPLC) pour les peptides
Pour l’analyse des peptides, la modalité la plus utilisée est la phase inverse (Reversed-Phase, RP-HPLC). Dans cette configuration :
- La phase stationnaire est apolaire (chaînes C18 liées à la silice)
- La phase mobile est polaire (gradient eau vers acétonitrile)
Les peptides, qui ont des régions à la fois polaires et apolaires, sont séparés en fonction de leur hydrophobicité : les peptides les plus hydrophiles sortent en premier, les plus hydrophobes après. Cette technique est excellente pour séparer le peptide cible des impuretés de synthèse, qui diffèrent souvent d’un ou de quelques acides aminés.
Comment lire un chromatogramme
Le résultat de l’analyse
Le résultat d’une analyse HPLC est un chromatogramme : un graphique avec le temps de rétention (minutes) sur l’axe X et l’intensité du signal UV (milli-absorbance, mAU) sur l’axe Y.
Éléments clés du chromatogramme
Le pic principal (Main Peak) : c’est le pic le plus haut et le plus proéminent du chromatogramme, correspondant au peptide cible. Sa position sur l’axe X est le temps de rétention — une valeur caractéristique qui dépend de la structure du peptide et des conditions analytiques. Pour une méthode HPLC donnée, le temps de rétention est reproductible et permet l’identification du composé.
Les pics d’impuretés : ce sont les pics plus petits qui apparaissent avant, après ou à côté du pic principal. Chaque pic correspond à une impureté différente — un peptide tronqué, une forme oxydée, un isomère ou un sous-produit de la synthèse.
La ligne de base : c’est la ligne horizontale du chromatogramme en l’absence de composés qui sortent. Une ligne de base stable et plate indique une analyse bien conduite.
L’aire du pic : la pureté se calcule comme :
Pureté (%) = (Aire du pic principal / Aire totale de tous les pics) x 100
Par exemple, si le pic principal a une aire de 990 unités et l’aire totale de tous les pics est de 1000 unités, la pureté est de 99,0 %.
Comment évaluer un chromatogramme de qualité
Un bon chromatogramme présente :
- Un pic principal symétrique : un pic asymétrique (avec une “queue” ou un “front”) peut indiquer des problèmes chromatographiques ou un mélange d’isomères
- Une ligne de base plate : des oscillations dans la ligne de base suggèrent des problèmes instrumentaux ou une contamination des solvants
- Une bonne résolution : les pics d’impuretés doivent être clairement séparés du pic principal
- Une échelle temporelle adéquate : le gradient doit être suffisamment long pour séparer les composants
Le système de classification de la pureté
Tous les peptides ne sont pas égaux. L’industrie utilise un système de classification basé sur la pureté HPLC :
Grades de pureté
| Grade | Pureté HPLC | Usage typique | Coût relatif |
|---|---|---|---|
| Crude (brut) | moins de 70 % | Non adapté à la recherche | Très bas |
| Research grade | plus de 95 % | Criblage initial, études préliminaires | Bas |
| High purity | plus de 98 % | Recherche standard, la plupart des études | Moyen |
| Premium | plus de 99 % | Études quantitatives précises, in vivo | Élevé |
| Ultra-premium | plus de 99,5 % | Études de référence, dose-réponse critiques | Très élevé |
Ce que ça signifie en pratique
La différence numérique entre 95 % et 99 % peut sembler modeste — seulement 4 points de pourcentage. Mais regardons ce que ça signifie en termes de contenu effectif :
Peptide à 95 % de pureté : sur 10 mg de poudre, 9,5 mg sont le peptide souhaité et 0,5 mg sont des impuretés. Si tu prépares une solution à 5 mg/ml, chaque millilitre contient 0,25 mg d’impuretés inconnues.
Peptide à 99 % de pureté : sur 10 mg de poudre, 9,9 mg sont le peptide souhaité et seulement 0,1 mg sont des impuretés — cinq fois moins par rapport à 95 %.
Peptide à 99,5 % de pureté : sur 10 mg de poudre, 9,95 mg sont le peptide souhaité et à peine 0,05 mg sont des impuretés — dix fois moins par rapport à 95 %.
Peptide à 99,8 % de pureté : sur 10 mg de poudre, 9,98 mg sont le peptide souhaité et seulement 0,02 mg sont des impuretés — vingt-cinq fois moins par rapport à 95 %.
Pourquoi la pureté compte : les raisons scientifiques
Les peptides comme le GLP-1 sont des messagers biologiques que ton corps produit déjà naturellement — par exemple, le GLP-1 est libéré après chaque repas pour signaler la satiété. Quand tu utilises une version synthétique comme le sémaglutide ou le TRIPLE-G, tu veux qu’elle soit le plus possible identique au signal naturel, sans “bruit” chimique.
1. Reproductibilité des résultats
Le principe fondamental de la science est la reproductibilité : une expérience menée dans les mêmes conditions doit produire les mêmes résultats. Les impuretés introduisent de la variabilité parce que :
- La composition et la concentration des impuretés varient d’un lot à l’autre
- Certaines impuretés peuvent avoir une activité biologique propre (agoniste ou antagoniste)
- Le “bruit” des impuretés masque le signal du peptide cible
Avec un peptide à 99,5 %+, la variabilité introduite par les impuretés est négligeable et les résultats sont hautement reproductibles.
2. Exactitude du dosage
Dans toute étude dose-réponse, la précision du dosage est critique. Si le peptide a une pureté de 95 %, chaque dose nominale contient effectivement 5 % de moins de principe actif par rapport à ce qui a été calculé. Pour des études qui mesurent des différences fines entre les dosages (par exemple, 100 mcg vs 250 mcg vs 500 mcg), cette imprécision peut :
- Déplacer la courbe dose-réponse
- Altérer la détermination de l’EC50
- Produire des données irreproductibles entre des personnes différentes utilisant des peptides de puretés différentes
3. Réduction des effets confondants
Les impuretés ne sont pas inertes. Elles peuvent :
- Générer des faux positifs : une impureté avec une activité biologique propre peut produire un effet attribué par erreur au peptide cible
- Causer une toxicité : les sous-produits de synthèse (agents de couplage résiduels, solvants) peuvent être cytotoxiques
- Interférer avec les dosages : des impuretés fluorescentes ou absorbant les UV peuvent interférer avec les dosages spectrophotométriques ou immunologiques
4. Dose effective inférieure nécessaire
Un corollaire pratique de la haute pureté est qu’il faut des doses nominales inférieures pour obtenir le même effet biologique. Un peptide à 99,8 % nécessite environ 5 % de moins de matériau par rapport à un peptide à 95 % pour obtenir la même concentration effective de principe actif. Cela peut se traduire par des économies significatives.
Impuretés courantes dans la synthèse peptidique
Origines des impuretés
La synthèse peptidique en phase solide (SPPS, Solid-Phase Peptide Synthesis) est un procédé chimique complexe dans lequel les acides aminés sont assemblés un par un sur un support solide. Chaque étape de couplage (ajout d’un acide aminé) a une efficacité inférieure à 100 %, générant des impuretés caractéristiques.
Types principaux d’impuretés
Peptides de délétion (Deletion Peptides) : ils se produisent quand un acide aminé n’est pas incorporé dans la séquence. Le résultat est un peptide auquel il manque un ou plusieurs résidus. Pour un peptide de 39 acides aminés comme le TRIPLE-G (retatrutide), la délétion d’un seul résidu produit un peptide avec un poids moléculaire inférieur d’environ 100-200 Da.
Peptides tronqués (Truncated Peptides) : la synthèse s’interrompt prématurément, générant des fragments de la séquence cible. Ce sont typiquement les impuretés principales dans les peptides de faible pureté.
Formes oxydées : la méthionine et le tryptophane peuvent s’oxyder durant la synthèse ou la purification. Le sulfoxyde de méthionine est l’impureté d’oxydation la plus courante.
Épimères (D-acides aminés) : durant le couplage, la racémisation partielle peut convertir les L-acides aminés en D-acides aminés, générant des diastéréomères du peptide cible.
Peptides désamidés : l’asparagine et la glutamine peuvent subir une désamidation, générant des impuretés avec une charge différente.
Résidus d’agents de couplage et de solvants : des traces de HBTU, HATU, DMF, NMP ou d’autres réactifs de synthèse peuvent co-purifier avec le peptide.
Quantification des impuretés
Un rapport HPLC complet identifie non seulement la pureté totale, mais aussi les impuretés individuelles avec leur abondance relative. Un rapport de haute qualité indique :
- Pureté du pic principal (%)
- Liste des impuretés détectables avec leur temps de rétention et leur abondance (%)
- Limite de détection de la méthode
- Conditions analytiques (colonne, gradient, détecteur)
Comment vérifier les déclarations de pureté
Le problème de l’autodéclaration
Le marché des peptides de recherche présente un problème structurel : beaucoup de fournisseurs déclarent des puretés élevées (99 %+) sans fournir de preuves analytiques vérifiables. Les déclarations de pureté non étayées par des données sont, dans le meilleur des cas, peu fiables.
Certificat d’analyse (CoA) interne
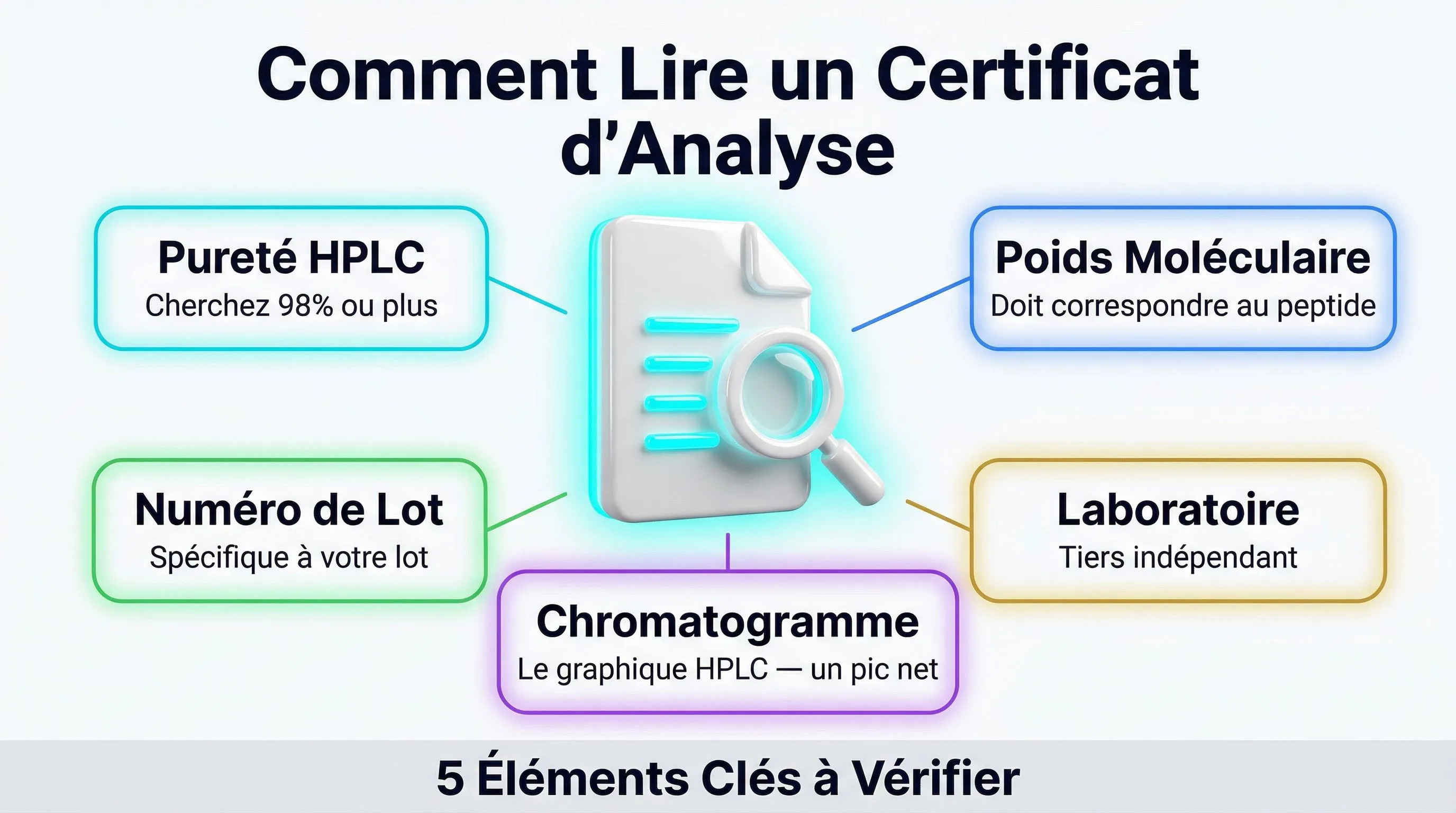
Le premier niveau de vérification est le Certificat d’Analyse (CoA) fourni par le producteur. Un CoA crédible doit inclure :
- Date de l’analyse
- Numéro de lot du peptide
- Méthode HPLC utilisée (type de colonne, gradient, longueur d’onde)
- Chromatogramme complet (pas seulement le chiffre de pureté)
- Résultat de la spectrométrie de masse (poids moléculaire mesuré vs théorique)
- Nom et signature de l’analyste ou du responsable qualité
Signaux d’alerte dans un CoA :
- Seulement le chiffre de pureté sans chromatogramme : la valeur pourrait être inventée
- Chromatogramme avec résolution basse ou échelle temporelle trop courte : des impuretés pourraient être masquées
- Absence de données de masse : l’identité du peptide n’est pas confirmée
- Format générique sans numéro de lot : il pourrait s’agir d’un template réutilisé
Tests de tiers : le standard de référence
Le moyen le plus fiable de vérifier la pureté d’un peptide est le test indépendant de tiers. Le laboratoire le plus respecté dans le secteur des peptides de recherche est Janoshik Analytical (République Tchèque), qui propose :
- Analyse HPLC avec chromatogramme complet
- Spectrométrie de masse pour confirmation de l’identité
- Rapport indépendant et impartial
- Résultats publiables et vérifiables
Un fournisseur qui soumet volontairement ses produits au test Janoshik démontre sa confiance dans la qualité de ses peptides. Au contraire, un fournisseur qui refuse ou décourage le test indépendant devrait susciter des soupçons.
Le test en interne
Les personnes ayant accès à un système HPLC peuvent vérifier en interne la pureté des peptides achetés. La méthode standard prévoit :
- Préparer une solution du peptide dans de l’eau ou de l’acétonitrile dilué
- Injecter 5-20 microlitres dans le système HPLC
- Utiliser une colonne C18 avec gradient linéaire eau/acétonitrile + 0,1 % TFA
- Détecter à 214 nm ou 220 nm
- Calculer la pureté à partir de l’intégration des aires des pics
Le compromis coût-pureté
Pourquoi la pureté coûte cher
Le prix d’un peptide augmente significativement avec la pureté requise pour une raison simple : la purification a un rendement décroissant. Pour obtenir un peptide à 99 %+ à partir du brut (environ 70 %), il faut :
- Purification HPLC préparative (la même technique analytique, mais à plus grande échelle)
- Sélection rigoureuse des fractions : seules les fractions centrales du pic, avec la pureté maximale, sont collectées
- Les fractions latérales (contenant des impuretés) sont éliminées : perte de matériau
- Pour atteindre 99,5 %+, une seconde purification peut être nécessaire : perte supplémentaire
Le résultat est qu’à partir de 100 mg de peptide brut, on pourrait obtenir :
| Pureté cible | Rendement typique | mg obtenus à partir de 100 mg brut |
|---|---|---|
| plus de 95 % | 50-70 % | 50-70 mg |
| plus de 98 % | 30-50 % | 30-50 mg |
| plus de 99 % | 20-35 % | 20-35 mg |
| plus de 99,5 % | 10-25 % | 10-25 mg |
| plus de 99,8 % | 5-15 % | 5-15 mg |
La perte de matériau dans la purification est le principal facteur de coût des peptides à haute pureté.
Quand ça vaut la peine d’investir dans la pureté
Le choix du grade de pureté dépend de l’application :
Plus de 95 % est suffisant pour :
- Le criblage initial de bibliothèques peptidiques
- Les études de liaison qualitatives (oui/non)
- La mise au point de méthodes analytiques
- Les expériences exploratoires
Plus de 98 % est recommandé pour :
- La plupart des études de recherche standard
- Les essais cellulaires in vitro
- Les études de liaison quantitatives
- Les études préliminaires d’activité biologique
Plus de 99 % est nécessaire pour :
- Les études dose-réponse précises
- Les expériences in vivo
- Les études de pharmacocinétique
- Les publications dans des revues à comité de lecture
Plus de 99,5 % est idéal pour :
- Les standards de référence
- Les études GLP (Good Laboratory Practice)
- La validation de méthodes analytiques
- La recherche destinée à appuyer des dossiers réglementaires
Pour approfondir comment lire un certificat d’analyse et comparer les puretés, sur fornitori europei specializzati tu trouveras des guides détaillés et des rapports Janoshik publiés pour chaque lot, avec des puretés dans la gamme ultra-premium (99,8 % ou plus).
Techniques complémentaires à l’HPLC
Spectrométrie de masse (MS)
Alors que l’HPLC mesure la pureté, la spectrométrie de masse confirme l’identité du peptide. Les deux techniques sont complémentaires :
- HPLC : répond à la question “quelle est sa pureté ?”
- MS : répond à la question “est-ce le bon peptide ?”
Les techniques MS les plus utilisées pour les peptides sont :
- ESI-MS (Electrospray Ionization) : la plus courante, génère des ions multicharges à partir du peptide
- MALDI-TOF (Matrix-Assisted Laser Desorption/Ionization - Time of Flight) : excellente pour les peptides et les protéines
- LC-MS (Liquid Chromatography - Mass Spectrometry) : combine HPLC et MS dans un seul instrument, permettant d’identifier chaque pic du chromatogramme
Analyse des acides aminés (AAA)
L’analyse des acides aminés hydrolyse le peptide en ses acides aminés constitutifs et les quantifie individuellement. Cela confirme :
- La composition en acides aminés du peptide
- Le contenu peptidique effectif (net du contre-ion et de l’eau)
- La stoechiométrie correcte des acides aminés
Test LAL pour les endotoxines
Pour les peptides destinés à des études in vivo ou à des dosages cellulaires sensibles, le test LAL (Limulus Amebocyte Lysate) est essentiel pour exclure la contamination par des endotoxines bactériennes (lipopolysaccharides). Les endotoxines peuvent :
- Activer le système immunitaire inné
- Altérer les résultats des dosages immunologiques
- Causer de la fièvre et un choc septique dans des études in vivo
Conservation et stabilité : comment protéger la pureté
Un peptide acheté à 99,8 % de pureté ne maintiendra pas cette pureté indéfiniment s’il n’est pas conservé correctement. Les principaux facteurs de dégradation sont :
Humidité
Les peptides lyophilisés sont hygroscopiques et absorbent l’eau de l’environnement. L’humidité accélère les réactions de dégradation (hydrolyse, désamidation). Conserve les peptides lyophilisés dans des contenants hermétiques, idéalement avec un sachet de gel de silice.
Température
Les réactions chimiques de dégradation doublent approximativement de vitesse pour chaque augmentation de 10 °C. Conserve les peptides à -20 °C pour un usage à moyen terme (mois) ou à -80 °C pour une conservation à long terme (années). Évite les cycles répétés de congélation-décongélation.
Lumière
Le rayonnement UV peut dégrader les acides aminés photosensibles (tryptophane, tyrosine). Conserve les peptides dans des flacons ambrés ou à l’abri de la lumière.
Oxydation
L’oxygène atmosphérique peut oxyder la méthionine, la cystéine et le tryptophane. Pour une conservation à long terme, considère la conservation sous atmosphère inerte (azote ou argon).
Peptides reconstitués
Une fois reconstitué en solution, la stabilité du peptide diminue significativement. Recommandations générales :
- Solutions aqueuses à 4 °C : stables pendant des jours à des semaines
- Solutions aqueuses à -20 °C : stables pendant des mois
- Subdivise en aliquotes pour éviter les cycles de congélation-décongélation
- Ajoute 0,1 % d’albumine sérique bovine (BSA) pour prévenir l’adsorption aux contenants à faibles concentrations
Conclusions
La pureté HPLC n’est pas un détail technique — c’est le paramètre fondamental qui détermine la qualité d’un peptide et, par conséquent, la validité des résultats qui en découlent. La différence entre un peptide à 95 % et un à 99,8 % se traduit par des différences concrètes dans la reproductibilité, l’exactitude du dosage et l’absence d’artefacts.
Cela vaut encore plus pour des molécules complexes comme le TRIPLE-G (retatrutide), avec ses 39 acides aminés : plus la chaîne est longue, plus les impuretés de synthèse potentielles sont nombreuses. Quand tu travailles avec un triple agoniste qui active trois récepteurs différents (GLP-1, GIP et glucagon), tu veux être sûr que ce que tu as dans le flacon est exactement ce que tu attends.
Pour ceux qui veulent approfondir, investir dans la qualité du matériau de départ est toujours plus efficace que chercher à comprendre pourquoi les résultats ne collent pas.
Références
- Mant CT, Hodges RS. “High-Performance Liquid Chromatography of Peptides and Proteins.” CRC Press. 1991.
- Rabel SR, Stobaugh JF. “Applications of capillary electrophoresis in pharmaceutical analysis.” Pharm Res. 1993.
- ICH Q6B. “Specifications: Test Procedures and Acceptance Criteria for Biotechnological/Biological Products.” International Council for Harmonisation, 2023.
- USP chapitre 621. “Chromatography.” United States Pharmacopeia, General Chapter.
- European Pharmacopoeia 11.0. “2.2.29. Liquid Chromatography.” Monographie générale.
- Coin I, et al. “Solid-phase peptide synthesis: from standard procedures to the synthesis of difficult sequences.” Nat Protoc. 2007;2(12):3247-3256.
- Janoshik Analytical Services. “Peptide Analysis Methodology.” Documentation technique.
Les informations contenues dans cet article sont destinées exclusivement à des fins éducatives et de recherche scientifique. Elles ne constituent pas un conseil professionnel sur la qualité des produits. Consulte toujours les lignes directrices et les protocoles de ton institution.
Questions Fréquentes
Qu'est-ce que la pureté HPLC d'un peptide et pourquoi est-elle importante ?
La pureté HPLC indique quel pourcentage de l’échantillon est constitué du peptide cible. Elle est mesurée par chromatographie liquide haute performance, qui sépare le peptide des impuretés. Une pureté élevée garantit des résultats reproductibles et un dosage précis en recherche.
Quelle est la différence concrète entre un peptide à 95 % et un à 99 % de pureté ?
Un peptide à 95 % contient 0,5 mg d’impuretés par flacon de 10 mg, tandis qu’un peptide à 99 % n’en contient que 0,1 mg, soit cinq fois moins. Cette différence impacte la reproductibilité des résultats et la précision du dosage dans les études de recherche.
Comment lire un chromatogramme HPLC sur un certificat d'analyse ?
Le pic principal (le plus haut) représente le peptide cible. Les petits pics sont les impuretés. La pureté se calcule en divisant l’aire du pic principal par l’aire totale de tous les pics. Un bon chromatogramme montre un pic principal symétrique et une ligne de base plate. Consulte notre guide sur les COA pour plus de détails.
Qu'est-ce que le test Janoshik pour les peptides de recherche ?
Janoshik Analytical est un laboratoire indépendant en République Tchèque spécialisé dans le test de peptides. Un fournisseur fiable qui soumet ses produits au test Janoshik démontre sa confiance dans leur qualité, car les résultats sont indépendants et impartiaux.
Quelle pureté HPLC minimum exiger lors de l'achat de peptides pour la recherche ?
Pour la recherche standard, une pureté HPLC d’au moins 98 % est recommandée. Pour les études dose-réponse et in vivo, viser 99 %+. Des fournisseurs européens vérifiés comme fornitori europei specializzati proposent des puretés HPLC de 99,8 %+ avec rapports Janoshik publiés pour chaque lot et livraison EU gratuite.